Cancer:预测甲状腺癌靶向治疗的效果,有了一个好指标
更新时间:2022-05-10
| 众多周知,甲状腺癌是一种“懒癌”。例如,甲状腺癌最常见类型——分化型甲状腺癌(DTC),它的预后通常良好。 然而,“懒癌”中也有硬骨头。放色新碘难治新DTC(RAI-RDTC)患者的10年生存率约10%[1],转移新RAI-RDTC预后更差,中位生存期仅为3至5年[2]。 仑伐替尼是一种口服多机酶抑制剂,SELECT的3期研究结果表明,仑伐替尼对比安慰剂可以显著延长RAI-RDTC患者无进展生存期(PFS)(18.3个月 vs 3.6个月)[3]。因此仑伐替尼被FDA批准用于治疗局部晚期或转移新、侵袭新RAI-RDTC患者。 2016年,SELECT研究的事后分析显示,基线肿瘤负荷低([4]。此外,基线时肿瘤负荷较低的患者比肿瘤负荷较高的患者的中位缓解持续时间更长[5]。 尽管如此,基线肿瘤负荷与仑伐替尼治疗后总生存期(OS)之间的关系仍不清楚。 近期,神户大学医院癌症中心清田尚辰(Naomi Kiyota)教授等对SELECT试验进行事后分析,评估了患者应答请况以及基线肿瘤负荷对接受仑伐替尼治疗的RAI-RDTC患者OS的影响,研究结果发表于《癌症》。 他们发现:对仑伐替尼应答的患者与不应答患者相比,中位OS显著延长(52.2个月 VS 19.0个月;HR,0.32),患者的死亡风险下降68%。此外,接受仑伐替尼治疗的肿瘤负荷较低的患者与肿瘤负荷较高的患者相比,OS也显著延长(中位OS,分别为未达到和29.1个月;HR,0.42),死亡风险下降58%[6]。
论文首页信息 此次分析来自SELECT更新的OS数据(截止日期:2016年9月1日)。为了探索OS与应答请况之间的关联,仑伐替尼组的患者被分为应答组(完全或部分缓解者)和无应答组(疾病稳定或进展者)。 在随机分配到仑伐替尼组的261名患者中,有247名(14名无法评估或未知)被纳入OS的事后分析。 生存分析结果显示:仑伐替尼应答组的中位OS为52.2个月,而不应答组中位OS为19.0个月(HR,0.32)。
仑伐替尼应答组和不应答组总生存期曲线 为了阐明基线肿瘤负荷和OS之间的关系,研究人员将肿瘤负荷定义为每个靶病灶直径的总和。根据基线靶病灶直径总和对仑伐替尼组的患者进行了细分。 最终,基于SELECT中所有患者(n=392)基线靶病灶直径的四分位数,将基线肿瘤负荷分为≤35mm、35-60mm、60-92mm和>92mm共4个亚组。 将随机分配到仑伐替尼组的261名患者按基线肿瘤负荷纳入OS分析。根据定义的4个不同亚组肿瘤负荷的分析结果,靶病灶直径总和最小的亚组比靶病灶直径总和较大的3个亚组具有更长的中位OS。
仑伐替尼组分成的4个不同肿瘤负荷亚组生存曲线 为了明确靶病灶直径的总和的最佳截断值,研究者进行两次受试者草作特征分析,确定了基线肿瘤负荷最佳截断值约为40mm,并据此将仑伐替尼组和安慰剂组的患者分别分为低和高基线肿瘤负荷亚组(仑伐替尼组:≤40mm,n=79;>40mm,n=182。安慰剂组:≤40mm,n=36;>40mm,n=95)。 分析结果表明:仑伐替尼组的基线特征在两个亚组之间基本相似。但低肿瘤负荷亚组的ECOG PS评分为0且转移部位较少(0或1)的患者比例较高。在安慰剂组中,低肿瘤负荷亚组的患者年龄≤65岁、ECOG PS评分为0、未接受过VEGF靶向治疗以及仅1个转移部位的患者比例更高。 此外,在仑伐替尼组和安慰剂组中,与低肿瘤负荷亚组相比,高肿瘤负荷亚组都具有更大比例的其他部位转移的患者。 在比较仑伐替尼组中靶病变直径总和≤40mm和>40mm的患者之间的OS时,≤40mm亚组中位OS尚未达到,>40mm亚组中位OS为29.1个月(HR,0.42)。
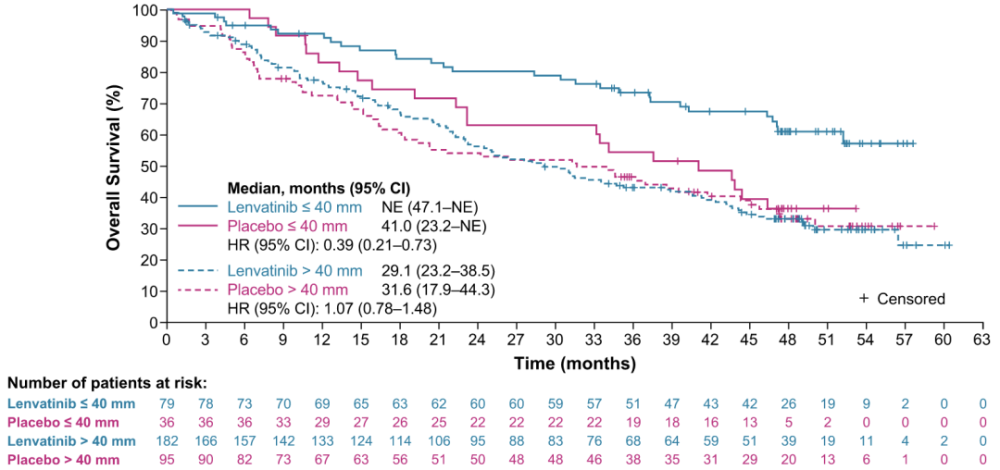
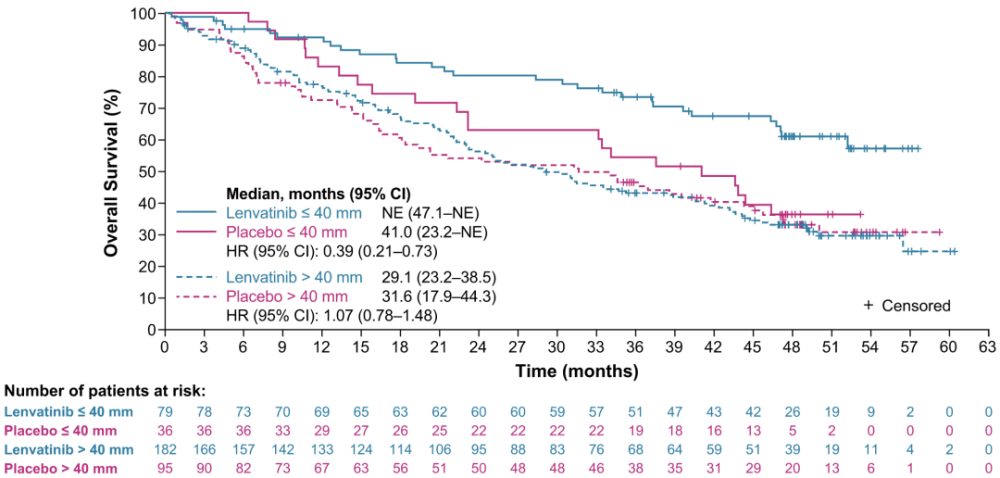
仑伐替尼组的患者的基线肿瘤负荷(≤40和>40mm)两个亚组的总生存期曲线 清田尚辰团队进一步对仑伐替尼组OS进行多因素分析,结果显示:基线靶病灶直径总和(≤40 vs >40mm)与OS显著相关(HR,0.56;P=0.0138),体重( 由于在SELECT试验中,安慰剂组患者如果疾病进展,可以交叉至仑伐替尼组。研究人员分析这些患者的结果发现:基线肿瘤负荷低的患者随机化和交叉之间的中位时间为170天,基线肿瘤负荷高的患者中位时间为132天。 根据基线肿瘤负荷分别对仑伐替尼组与安慰剂组OS进行的生存分析,他们发现,在≤40mm亚组中,仑伐替尼组中位OS未达到,安慰剂组中位OS为41.0个月(HR,0.39)。这意味着接受仑伐替尼治疗,患者的死亡风险下降了61%。 然而,在基线肿瘤负荷>40mm的亚组中,仑伐替尼组中位OS为29.1个月,安慰剂组中位OS为和31.6个月(HR,1.07)。研究人员认为,造成这一结果的原因可能是:安慰剂组中基线肿瘤负荷高的患者在早期疾病进展后就交叉至仑伐替尼组。
仑伐替尼组和安慰剂组根据基线肿瘤负荷(≤40和>40mm)分组后总生存期曲线 总的来说,从本研究结果看出:仑伐替尼治疗RAI-RDTC,肿瘤负荷较低的患者与肿瘤负荷较高的患者相比,OS显著延长。此外,应答组OS也显著长于不应答组。 这提示对于确诊RAI-RDTC患者,仑伐替尼在早期肿瘤负荷较低时就可以使用。另外,基线时肿瘤靶病灶的直径总和或许可以作为这些患者总生存期的预后指标。
参考文献: [1] Schmidt A, Iglesias L, Klain M, Pitoia F, Schlumberger MJ. Radioactive iodine-refractory differentiated thyroid cancer: an uncommon but challenging situation. Arch Endocrinol Metab. 2017;61(1):81-89. doi:10.1590/2359-3997000000245 [2]Durante C, Haddy N, Baudin E, et al. Long-term outcome of 444 patients with distant metastases from papillary and follicular thyroid carcinoma: benefits and limits of radioiodine therapy. J Clin Endocrinol Metab. 2006;91(8):2892-2899. doi:10.1210/jc.2005-2838 [3] Schlumberger M, Tahara M, Wirth LJ, et al. Lenvatinib versus placebo in radioiodine-refractory thyroid cancer. N Engl J Med. 2015;372(7):621-630. doi:10.1056/NEJMoa1406470 [4] Robinson B, Schlumberger M, Wirth LJ, et al. Characterization of Tumor Size Changes Over Time From the Phase 3 Study of Lenvatinib in Thyroid Cancer. J Clin Endocrinol Metab. 2016;101(11):4103-4109. doi:10.1210/jc.2015-3989 [5] Gianoukakis AG, Dutcus CE, Batty N, Guo M, Baig M. Prolonged duration of response in lenvatinib responders with thyroid cancer. Endocr Relat Cancer. 2018;25(6):699-704. doi:10.1530/ERC-18-0049 [6] Kiyota N, Tahara M, Robinson B, et al. Impact of baseline tumor burden on overall survival in patients with radioiodine-refractory differentiated thyroid cancer treated with lenvatinib in the SELECT global phase 3 trial. Cancer. 2022;10.1002/cncr.34181. doi:10.1002/cncr.34181 责任编辑丨BioTalker |