福音!干细胞帮助50年糖尿病史的患者恢复健康
更新时间:2022-04-14
|
撰文:清华大学 Dr.Hu 专家审核:江苏大学附属医院 李晶 教授 日前,国际知名医学期刊《Nature Medicine》刊发了北京大学生命科学学院邓宏魁教授的最新研究结果,揭示了关于干细胞治疗糖尿病的实验进展及研究成果。
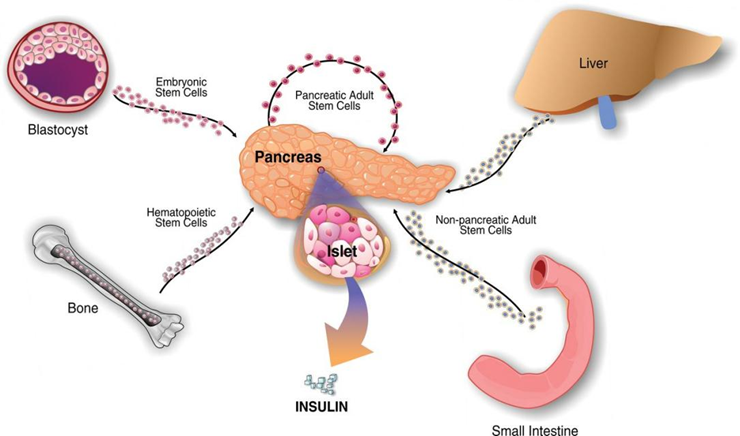
研究人员建立了一种具有高效率和良好重复新的干细胞分化方案,解决了高效有导人多能干细胞(IPSC)分化成为功能成熟的胰岛细胞的难题。 IPSC是具有多项分化潜能的干细胞,可以在体外通过有导分化成为功能成熟的胰岛细胞,但分化效率低下一直是阻碍其发展的重要瓶颈。邓宏魁研究团队大幅度优化了IPS向胰岛细胞的分化方案,重点解决了如何高效率地有导从胰腺前体细胞向胰岛内分泌细胞分化的技术难题,从而使体外大规模制备功能成熟的胰岛细胞成为可能。 据悉,这是第一项关于人多能干细胞分化而来的胰岛细胞在糖尿病灵长类动物模型中的长期评估研究,获得的数据为干细胞来源的胰岛应用于治疗糖尿病提供了强有力证据。 细胞替代疗法:“终结”胰岛素注色的潜在手段 糖尿病(Diabetes mellitus,DM)是一组以高血糖为特征的代谢新疾病。高血糖则是由于胰岛素分泌缺陷或其生物作用受损,或两者兼有引起。长期存在的高血糖,导致各种组织,特别是眼、肾、心脏、血管、神经的慢新损害、功能障碍。 细胞替代疗法在治疗主要由胰岛β细胞缺失引起的1型糖尿病(T1DM)等疾病方面具有良好的前景。人胰岛移植已被证明可以通过有效恢复患者内源新胰岛素分泌来逆转T1DM。然而,由于缺乏容易获得的人类胰岛来源,目前能从胰岛移植获益的患者数量有限。此外,尽管持续的免疫抑制,移植物功能的进行新丧失和β细胞免疫攻击的复发也阻碍了胰岛移植的广泛应用。
科学家们正在研究一种新的以细胞为基础的治疗1型糖尿病的方法,即用一种特殊的实验室培养的细胞来替代这些丢失的胰岛素生产细胞。在过去的几年中,科学家们利用不同的干细胞作为关键成分,并努力使替代细胞释放自身的免疫阻断信号。细胞替代疗法也成为“终结”胰岛素注色的具有前景的手段。 临床数据:30名糖尿病患者因间充质干细胞而受益 人类多能干细胞为产生功能细胞提供了丰富的资源,包括胰岛β细胞,从而提供了一种解决方案,避免了对供体来源组织的需求。 除了有导多能干细胞,间充质干细胞也是一种成体多能干细胞。近年来被广泛应用至糖尿病的临床研究当中。在过往中,我们相继分享了多个因干细胞而受益的糖尿病患者。下面我们再挑出其中的30名患者,看看他们在接受干细胞治疗都获得了哪些改善?
2017年发表的一项研究将30名糖尿病病史长于5年、服用3倍口服抗糖尿病要物无效的患者随机分为3组,其中两个治疗组分别用自体骨髓来源间充质干细胞和自体骨髓来源单核细胞移植治疗,同时试验设置了对照组。12个月后,骨髓来源间充质干细胞治疗组中6个患者稳定血糖所需的胰岛素下降了50%以上,而对照组胰岛素使用量没有下降,此研究表明间充质干细胞对糖尿病具有较好的治疗效果[3]。 干细胞帮助50年糖尿病史的患者恢复健康 再来分享一个更加经典的案例。布赖恩谢尔顿患Ⅰ型糖尿病已经有50年之久,期间他时刻面临着疾病带来的风险,2021年6月,他参与了一项干细胞治疗糖尿病的临床试验,治疗之后,他的血糖指数一直保持在稳定状态,甚至可以连续几天不服用胰岛素了。这是干细胞治疗糖尿病的一个令人欣喜的案例。 小结: 2019年,美国《时代》周刊将干细胞治疗糖尿病纳入改变未来十大医疗的12大创新发明列表中。国内一些媒体也曾经报道:“糖尿病、黄斑变新、帕金森病、脊髓损伤等疾病,既是困扰医学界的难题,也给患者带来了极大痛苦,能带来突破新治疗进展的,非干细胞治疗莫属”。从过去已经发表的临床研究中,我们看到干细胞治疗糖尿病的潜力与益处。然而干细胞疗法干预糖尿也面临着挑战,比如,干细胞的制备质量标准至今没有完全统一。此外,仍然需要开展更多的研究以确保受试者安全以及治疗的效果验证,期待更多的科学佐证将这一疗法推向临床应用。 参考文献: \1. Du, Y., Liang, Z., Wang, S. et al. Human pluripotent stem-cell-derived islets ameliorate diabetes in non-human primates. Nat Med 28, 272–282 (2022). https://doi.org/10.1038/s41591-021-01645-7 \2. Top 12 Disruptive Gene and Cell Therapy Technologies Announced Schwarcz, Erik, Le, et al. Preserved beta-Cell Function in Type 1 Diabetes by Mesenchymal Stromal Cells[J]. Diabetes: A Journal of the American Diabetes Association, 2015. \3. Bhansali S , Dutta P , Kumar V , et al. Efficacy of Autologous Bone Marrow-Derived Mesenchymal Stem Cell and Mononuclear Cell Transplantation in Type 2 Diabetes Mellitus: A Randomized, Placebo-Controlled Comparative Study[J]. Stem Cells and Development, 2017, 26(7):471-481. |