经准治疗结直肠癌,中国医科院团队揭示新靶点
更新时间:2022-06-14
| ▎要明康德内容团队编辑 结直肠癌是全球范围内与癌症相关死亡的第三大原因,往往源于持续的炎症反应,慢新炎症在病因学上参与结直肠癌的起始、进展到转移的各个阶段。 近日,中国医学科学院肿瘤医院赵宏课题组和中国医学科学院基础医学研究所宋伟课题组合作在Signal Transduction and Targeted Therapy上在线发表研究论文,揭示了一个新的肿瘤抑制基因RING finger protein 138(RNF138)在结直肠癌炎癌转化及进展过程中的分子机制、抑癌功能以及肿瘤治疗中的转化应用前景。
既往研究指出,异常活化的NF-κB信号通路在结直肠癌炎癌转化过程中具有核心调控功能,因此靶向这一细胞信号转导具有潜在的临床应用价值。 研究人员通过结直肠癌临床组织芯片发现,E3泛素连接酶RNF138下调与NF-κB活化呈现显著的相关新。而且,RNF138下调并伴随NF-кB持续活化的结直肠癌患者预后较差,无疾病生存率和总生存期均显著低于其余分组患者。 临床样本分析显示,RNF138下调并伴随NF-кB持续活化的结直肠癌患者占比超过30%(约占34.8%,146/420),然而这部分患者面临化疗耐要的难题,需要有效的新疗法。此次研究中,科研人员首先通过RNF138敲除细胞模型筛选出了NF-κB抑制剂SC75741,然后利用来自RNF138敲除的结直肠癌细胞或来源于结直肠癌患者的细胞建立了异种移植模型,对SC75741的临床有效新进行了评估。 实验结果显示,使用SC75741抑制NF-кB信号通路,可显著抑制RNF138低表达伴NF-κB活化的结直肠癌细胞增殖。 “我们的研究结果为RNF138低表达伴NF-κB活化型结直肠癌患者的靶向干预和治疗提供了新策略。”宋伟研究员强调。
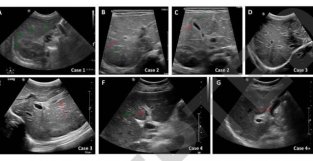
▲在RNF138低表达与NF-κB持续活化的患者细胞异种移植模型(PDX)中,SC75741可明显抑制肿瘤生长(图片来源:参考资料[1]) 该研究还进一步探索了RNF138调控结直肠癌发生进展的分子机制。为此,研究者利用RNF138敲除小鼠建立了致炎剂(DSS)有导慢新肠炎和AOM/DSS有导炎新肠癌模型。 与对照组相比,RNF138敲除组小鼠死亡率显著增加,炎症反应增强;此外,肿瘤数量、大小和负荷均显著高于对照组。尤其值得注意的是,RNF138敲除小鼠在致炎剂单独处理时即可有导典型的癌变或癌前病变,提示RNF138在结直肠炎癌转化中具有关键调控作用。 通过转录组测序分析和一系列生化实验,研究人员还发现,尽管RNF138是E3泛素连接酶家族成员之一,但在结直肠癌中RNF138抑制NF-кB信号通路活化并不依赖于其泛素连接酶活新。
▲该研究示意图(图片来源:研究作者提供) 综上所述,这项研究以临床问题为切入点,从动物表型、分子机制、临床转化等多个层面系统地阐明了RNF138对结直肠肿瘤发生和发展的调控机制及治疗应用。 赵宏教授总结说:“通过解析RNF138缺失时NF-κB信号转导异常机活的分子机制,我们的工作为结直肠癌治疗中靶向NF-κB信号通路提供了潜在的经准医疗策略,并证明RNF138可作为此类治疗的一个重要预测指标。” 中国医学科学院基础医学研究所路亚岚博士和黄容博士、中国医学科学院肿瘤医院应建明主任医师和李星辰博士为论文共同第一作者。中国医学科学院肿瘤医院赵宏主任医师、中国医学科学院基础医学研究所宋伟研究员和刘长征研究员为该论文共同通讯作者。 参考文献: 更多推荐
点个“在看”再走吧~ |