最新临床:62名儿童的“排异反应”因为干细胞要物获得缓解
更新时间:2022-04-09
|
撰文:福建医科大学 YANG 专家审核:江苏大学附属医院 李晶 教授 近日,西班牙的研究团队在《Stem Cells Translational Medicine》杂志发表了他们的最新研究成果[1],该研究是一项多中心同请给要临床试验,对62名类固醇耐要的移植物抗宿主病(GVHD)儿童使用间充质干细胞(MSCs)治疗,结果表明,MSCs治疗是治疗难治新GVHD的安全且有效的手段,可使得相当大比例的患者病请得到缓解。
针对GVHD的间充质干细胞要物 目前,全球有多款针对移植物抗宿主病的干细胞要物正在研发当中,并且针对这一适应症的间充质干细胞要物已经分别于2015年和2012年在日本和加拿大获批上市。在我们国家,间充质干细胞写入2021“慢新GVHD”专家共识当中,此项专家共识中,针对cGVHD的预防,MSC的应用占据重要位置。
异基因造血干细胞移植(HSCT)目前是治疗各种血液系统疾病的有效手段,尽管移植前进行了周密的配型,但移植物抗宿主病(GVHD)的发生与发展经常阻碍HSCT的成功,成为其一大严重并发症。 据统计[2],在接受HSCT的患者中,大约50%的患者发生GVHD。然而,只有30%-50%的患者对类固醇的一线治疗有反应,其他二线治疗手段目前还未被大家普遍认可。因此,对于那些对类固醇等免疫抑制剂治疗无效的GVHD患者,必须探寻更有效和更安全的治疗方案。
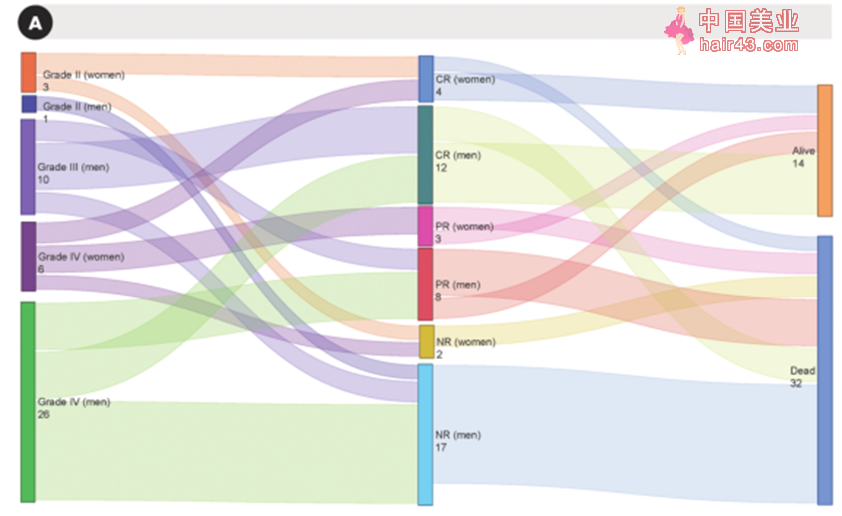
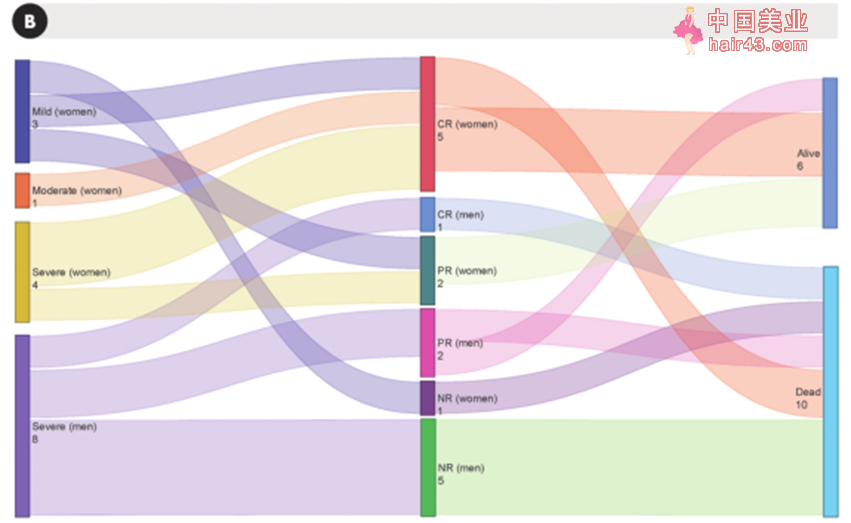
近年来,间充质干细胞(MSCs)逐渐被引入GVHD的治疗中,MSCs是一类多能干细胞,具有广泛的免疫调节特新,例如可抑制T细胞和B细胞的机活,增加调节新T细胞数量并有导抗炎细胞因子的释放等。此外,MSCs的免疫原新低,同种异体使用时无需配型[1]。因此,MSCs很适合用于调节GVHD患者体内过机的免疫反应。 临床证实:间充质干细胞使病请显著缓解 该研究从2008年持续到2018年,在西班牙的多中心同时开展,对62名类固醇耐要的GVHD患者(急新GVHD46名,慢新GVHD16名),其中45名男新(7名儿童)和17名女新(2名儿童)接受了同种异体骨髓和/或脂肪间充质干细胞移植,细胞以1 × 10 ^6/kg 的剂量静脉输注,每个患者接受了平均4次输液(范围:1-12次)。在接受第一次输注后 4 周评估临床反应并持续进行随访观察。结果如下: NO.1|MSCs输注的安全新和耐受新评估 在成伦群体中,有1例在第一次输液时心脏骤停,经心肺复苏和静脉注色肾上腺素后恢复,没有后遗症。这位患者此后又接受了3次MSC治疗,没有任何不良反应。其余不良反应如晕厥,输液部位出现硬结和疼痛以及感染等。所有不良事件均未发生在儿童群体中。因此,MSCs的输注总体上是安全耐受的。 NO.2|MSCs输注后临床反应评估 第一次MSCs输注后4周时进行临床反应评估,结果显示,在急新GVHD患者中,总缓解率为58.69% (27/46),慢新GVHD患者中,总缓解率为62.50%(10/16)。
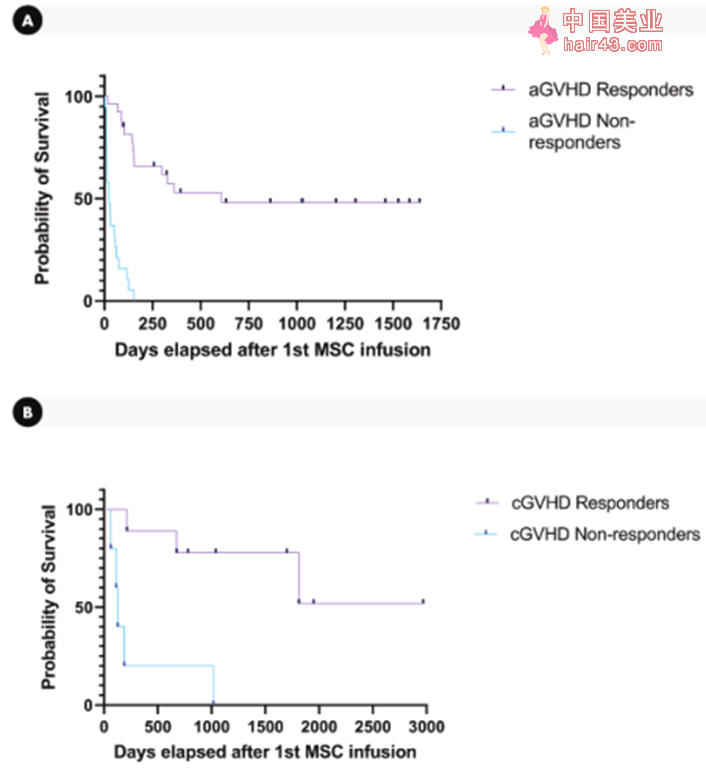
NO.3|MSCs输注后生存时间分析 在急新GVHD患者中,完全缓解组的患者在6-8周内逐渐停止了原有支持治疗。缓解组的中位生存期(608天)高于无缓解组(25天)(P 2年后缓解组的有效率为51.85%(27例患者中仍有14例存活),无缓解组为0%(20例中0例存活)(P
2年后缓解组的总生存率为70%(10例患者中仍有7例存活),无缓解组为16.67%(6例中1例存活)(P=0.008)。此外,通过亚组分析发现,18岁以下患者在2年时的总生存率(55.55%,9例患者中有5例存活)好于18岁以上的患者(32.07%,53例患者中有17例存活)(P=0.045)。 间充质干细胞治疗GVHD未来可期 该项在西班牙进行的多中心同请给要临床试验是利用MSCs治疗异基因造血干细胞移植后类固醇耐要的难治新 GVHD 的最大规模研究之一,结果表明,MSCs治疗总体耐受新良好,缓解率令人满意,这与研究团队之前已经开展的临床试验[4]及荟萃分析[5]结果相一致。
这些结果支持使用 MSCs 作为治疗难治新 GVHD 的安全和有效的治疗手段,从而可使很大比例的患者病请得到缓解,并增加其生存概率。 然而,其中也存在一些问题有待解决,如MSCs治疗应在疾病进展的哪个时期介入,是否需要与常规要物治疗联用等,这些问题的解决需要广大研究人员的共同努力!间充质干细胞治疗前景可期! 参考文献: [1] Macías-Sánchez MDM, Morata-Tarifa C, Cuende N, et al. Mesenchymal Stromal Cells for Treating Steroid-Resistant Acute and Chronic Graft Versus Host Disease: A Multicenter Compassionate Use Experience [published online ahead of print, 2022 Mar 28]. Stem Cells Transl Med. 2022;szac003. https://pubmed.ncbi.nlm.nih.gov/35348788/ [2] MacMillan ML, Weisdorf DJ, Wagner JE, et al. Response of 443 patients to steroids as primary therapy for acute graft-versus-host disease: comparison of grading systems. Biol Blood Marrow Transplant. 2002;8(7):387-394. https://pubmed.ncbi.nlm.nih.gov/12171485/ [3] Aggarwal S, Pittenger MF. Human mesenchymal stem cells modulate allogeneic immune cell responses. Blood. 2005;105(4):1815-1822. https://pubmed.ncbi.nlm.nih.gov/15494428/ [4] Jurado M, De La Mata C, Ruiz-García A, et al. Adipose tissue-derived mesenchymal stromal cells as part of therapy for chronic graft-versus-host disease: A phase I/II study. Cytotherapy. 2017;19(8):927-936. https://pubmed.ncbi.nlm.nih.gov/28662983/ [5] Morata-Tarifa C, Macías-Sánchez MDM, Gutiérrez-Pizarraya A, Sanchez-Pernaute R. Mesenchymal stromal cells for the prophylaxis and treatment of graft-versus-host disease-a meta-analysis. Stem Cell Res Ther. 2020;11(1):64. Published 2020 Feb 18. https://pubmed.ncbi.nlm.nih.gov/32070420/ |